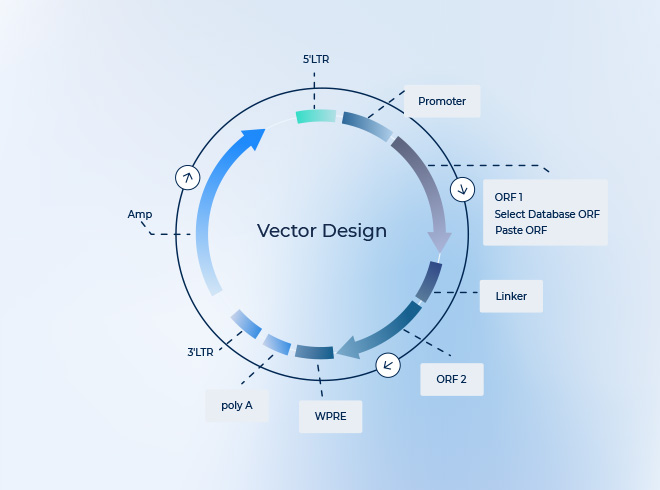
현대 신경과학 연구에서 외래 유전자를 표적 신경세포에 효율적이고 안정적이며 비교적 안전하게 전달하는 것은 뇌 기능 규명, 신경회로 연구, 질환 중재를 추진하는 핵심 기반입니다. 아데노부속바이러스(Adeno-Associated Virus, AAV)는 우수한 안전성, 낮은 면역원성, 신경계에 대한 높은 적합성, 그리고 유연한 공학적 개량 가능성으로 인해 신경과학 분야에서 가장 널리 사용되는 바이러스 벡터 중 하나로 자리 잡았습니다.
기초연구에서 중개의학에 이르기까지, AAV는 뉴런 표지, 신경활동 기록, 광유전학적 조절, 신경회로 추적, 신경계 질환 유전자치료 등에서 폭넓은 활용 가치를 보여주고 있습니다. 다시 말해, AAV는 신경과학 연구 도구 개발과 임상 응용 탐색을 연결하는 중요한 플랫폼이 되었습니다.
AAV가 신경과학 연구에 적합한 이유
1. 비교적 높은 안전성과 낮은 면역원성
AAV는 일반적으로 병원성이 낮은 바이러스 벡터로 간주되며, 대부분의 연구 및 임상 적용 환경에서 우수한 생물학적 안전성을 보입니다. 아데노바이러스나 렌티바이러스와 같은 다른 대표적 바이러스 벡터와 비교할 때, AAV는 염증 반응과 세포독성이 상대적으로 낮아 미세환경 변화에 민감한 중추신경계에 특히 적합합니다.
다만, AAV의 안전성은 투여 용량, 투여 경로, 숙주의 면역 상태와 밀접하게 연관되어 있습니다. 고용량 또는 전신 투여 조건에서는 잠재적인 면역반응 및 장기 독성 위험을 충분히 고려해야 합니다.
2. 뉴런에서의 장기적이고 안정적인 발현
뉴런은 말단분화세포로서 세포분열 활성이 매우 낮습니다. AAV는 이러한 세포 내에서 일반적으로 비통합성 환형 DNA(episome) 형태로 존재하며, 숙주 게놈을 크게 교란하지 않으면서 장기간 안정적인 유전자 발현을 유도할 수 있습니다.
이 특성은 학습과 기억 기전, 신경발달 과정, 만성 신경퇴행성 질환 모델, 장기 행동연구와 같이 장기 관찰이 필요한 연구에서 매우 중요합니다.
3. 다양한 혈청형을 통한 다차원적 전달 최적화
서로 다른 AAV 혈청형은 중추신경계에서 형질도입 효율, 세포 지향성, 축삭 수송 능력에 있어 뚜렷한 차이를 보입니다. 따라서 연구자는 실험 목적에 따라 적절한 혈청형을 선택하여 특정 뇌영역, 뉴런 아형, 또는 교세포에 대한 정밀 전달을 구현할 수 있습니다.
AAV1, 2, 5, 6, 8, 9 등을 비교한 체계적 연구는 뇌영역 및 세포 유형별 벡터 선택에 중요한 참고 근거를 제공하고 있습니다.
4. 세포 유형 특이적 발현 시스템과의 높은 호환성
AAV는 단순한 전달 도구를 넘어, 분자 설계를 통해 고정밀 발현 조절이 가능합니다. 예를 들면 다음과 같습니다.
- 세포 유형 특이적 프로모터(뉴런 특이적, 교세포 특이적 등)와 결합하여 표적화 발현 구현
- Cre/Flp 재조합 시스템과 결합하여 조건부 발현 조절 수행
- 인핸서 요소를 도입하여 특정 뉴런 아형에서의 발현 특이성 향상
이러한 전략을 통해 흥분성 뉴런, 억제성 뉴런, 다양한 교세포 집단을 정밀하게 조절할 수 있습니다.
신경과학에서의 AAV 대표 응용
1. 뉴런 표지 및 형태 분석
AAV는 GFP, mCherry와 같은 형광단백질 전달에 널리 활용되며, 이를 통해 뉴런의 세포체, 수상돌기, 축삭 투사를 시각화할 수 있습니다. 이는 뇌영역 구조 분석, 뉴런 형태 재구성, 투사 경로 매핑에 폭넓게 사용됩니다.
2. 신경활동 기록
GCaMP와 같은 유전자 암호화 칼슘 센서를 전달함으로써, AAV는 생체 내에서 신경세포 집단의 활동을 동적으로 모니터링할 수 있게 합니다. 이는 감각 정보 처리, 학습과 기억, 사회적 행동, 질환 관련 신경활동 변화 연구의 핵심 도구가 되었습니다.
3. 광유전학 및 화학유전학적 조절
AAV는 다양한 기능성 분자를 전달하여 신경활동의 정밀 조절을 가능하게 합니다.
- 광유전학 도구(ChR2, Arch, Halo 등): 밀리초 단위의 정밀 제어
- 화학유전학 도구(DREADDs 등): 보다 완화되고 지속적인 조절
이들 기술은 신경회로의 인과관계 규명에 큰 진전을 가져왔습니다.
4. 신경회로 추적
공학적으로 개량된 AAV(예: AAV2-retro)는 투사 뉴런에 대한 고효율 역행성 표지를 가능하게 하여, 입력원 뉴런을 확인하는 데 활용됩니다.
다만 AAV는 일반적으로 비시냅스성 추적에 사용되며, 시냅스를 넘어서는 신경회로 추적은 보통 개조 광견병바이러스 등 다른 바이러스 시스템과의 조합이 필요합니다.
5. 신경계 질환 연구 및 유전자치료
AAV의 신경계 질환 적용은 점차 성숙해지고 있으며, 대표적으로 파킨슨병, 척수성 근위축증, 유전성 망막질환 등이 포함됩니다. 이미 일부 임상연구에서는 AAV 매개 유전자 전달이 우수한 안전성과 초기 효능을 보여, 임상 전환 가능성을 시사하고 있습니다.
공학적 AAV가 신경과학 연구의 경계를 확장하다
최근 AAV의 공학적 개량은 신경계 내 전달 효율과 표적 특이성을 크게 향상시켰습니다.
- 지향진화와 캡시드 개량을 통한 고효율 뇌 전달 변이체 선별
- 역행성 전달, 혈액-뇌 장벽 통과, 세포 유형 특이적 표적화를 지원하는 신규 벡터 개발
예를 들어 AAV-PHP.B 및 그 유래 변이체는 특정 마우스 계통(C57BL/6 등)에서 광범위한 중추신경계 전달 능력을 보이는 것으로 보고되었습니다. 그러나 이러한 특성은 영장류 및 인간 유래 시스템에서는 제한적으로 나타나며, 뚜렷한 종 간 차이가 존재함을 시사합니다. 따라서 실험 설계와 결과 해석, 그리고 종 간 외삽에는 신중한 평가가 필요합니다.
AAV의 한계
AAV는 폭넓게 활용되고 있지만, 다음과 같은 한계도 존재합니다.
- 제한된 적재 용량: 약 4.7 kb 수준으로, 대형 유전자나 복잡한 발현 시스템 구축에 제약이 있음
(dual-AAV, split-intein 등의 전략으로 일부 보완 가능) - 뚜렷한 종 간 차이: 마우스에서 높은 효율을 보인 결과가 영장류나 인간 시스템에 그대로 적용되지는 않을 수 있음
- 면역 관련 위험: 고용량 또는 전신 투여 시 면역반응이나 장기 독성이 유발될 가능성이 있음
따라서 실험 설계 시에는 탑재 유전자의 크기, 혈청형 선택, 표적 세포 유형, 발현 기간, 투여 방식, 실험 동물 종 등을 종합적으로 고려해야 합니다.
맺음말
AAV는 안전성, 발현 안정성, 신경계 적합성 사이에서 우수한 균형을 이루고 있어, 신경과학 연구에서 대체하기 어려운 핵심 도구로 자리매김하고 있습니다. 뉴런 표지, 기능 기록, 회로 조절, 회로 추적, 유전자치료에 이르는 폭넓은 활용은 기초연구와 임상 전환을 연결하는 중요한 가교로서의 위치를 확립해 주었습니다.
앞으로 새로운 캡시드 설계, 세포 유형 특이적 조절 요소, 정밀 전달 전략이 지속적으로 발전함에 따라, AAV의 신경과학 분야 응용 범위는 더욱 확장될 것이며 보다 중요한 역할을 수행하게 될 것입니다.
References
1.Burger C, et al. Recombinant AAV viral vectors pseudotyped with viral capsids from serotypes 1, 2, and 5 display differential efficiency and cell tropism after delivery to different regions of the central nervous system. Molecular Therapy. 2004.
2.Aschauer DF, Kreuz S, Rumpel S. Analysis of transduction efficiency, tropism and axonal transport of AAV serotypes 1, 2, 5, 6, 8 and 9 in the mouse brain. PLoS One. 2013.
3.Tervo DGR, et al. A Designer AAV Variant Permits Efficient Retrograde Access to Projection Neurons. Neuron. 2016.
4.Deverman BE, et al. Cre-dependent selection yields AAV variants for widespread gene transfer to the adult brain. Nature Biotechnology. 2016.
5.Chan KY, et al. Engineered AAVs for efficient noninvasive gene delivery to the central and peripheral nervous systems. Nature Neuroscience. 2017.
6.Dimidschstein J, et al. A viral strategy for targeting and manipulating interneurons across vertebrate species. Nature Neuroscience. 2016.
7.Challis RC, et al. Systemic AAV vectors for widespread and targeted gene delivery in rodents. Nature Protocols. 2019.
8.Kaplitt MG, et al. Safety and tolerability of gene therapy with an adeno-associated virus (AAV) borne GAD gene for Parkinson’s disease: an open label, phase I trial. Lancet. 2007.
9.Hocquemiller M, et al. Adeno-Associated Virus-Based Gene Therapy for CNS Diseases. Human Gene Therapy. 2016.
10.Foust KD, et al. Intravascular AAV9 preferentially targets neonatal neurons and adult astrocytes. Nature Biotechnology. 2009.
About PackGene
PackGene Biotech is a world-leading CRO and CDMO, excelling in AAV vectors, mRNA, plasmid DNA, and lentiviral vector solutions. Our comprehensive offerings span from vector design and construction to AAV, lentivirus, and mRNA services. With a sharp focus on early-stage drug discovery, preclinical development, and cell and gene therapy trials, we deliver cost-effective, dependable, and scalable production solutions. Leveraging our groundbreaking π-alpha 293 AAV high-yield platform, we amplify AAV production by up to 10-fold, yielding up to 1e+17vg per batch to meet diverse commercial and clinical project needs. Moreover, our tailored mRNA and LNP products and services cater to every stage of drug and vaccine development, from research to GMP production, providing a seamless, end-to-end solution.